Ecco come gli antivirali e gli antireumatoidi curano i contagiati
I protocolli in atto negli ospedali italiani funzionano e fanno scuola nel resto del mondo. Via libera alla sperimentazione dell'antireumatoide Tocilizumab
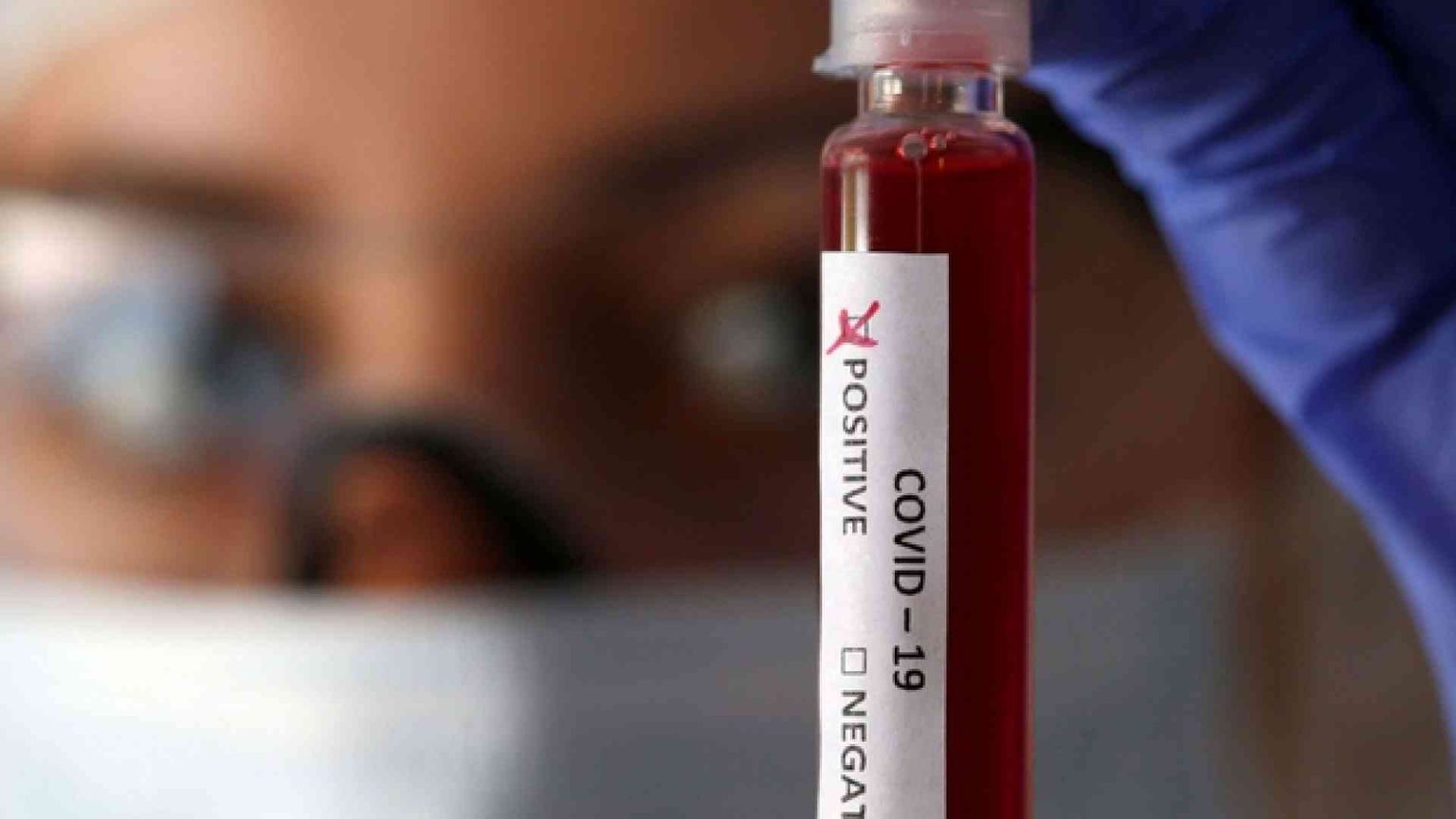
Si procede per tentativi, per ora. Ma i tentativi salvano vite. E allora rimbalzano sul web, volano sulle scrivanie dei colleghi dall'altra parte del mondo, diventano oggetto di studi, ricerche, sperimentazioni. La battaglia della scienza contro il coronavirus si combatte in corsia, con quel che c'è, in attesa che dai laboratori arrivi un vaccino.
In Italia è iniziata prima dell'epidemia, quando a fine gennaio la coppia di coniugi cinesi arrivati da Wuhan sono stati ricoverati - primi casi di Covid-19 in Italia - allo Spallanzani di Roma. Gravi, tutti e due, con febbre e polmonite. Anziani. L'unica strada percorribile, in quel momento, per provare a contenere l'infezione era quella degli antivirali: farmaci scoperti e utilizzati in passato contro altri virus e utilizzati già per la Sars e la Mers con qualche (piccolo) risultato. Con gli antivirali oggi - per cui l'Agenzia italiana del farmaco (Aifa) ha autorizzato l'uso off label, cioè slegato dalle indicazioni originarie - vengono curati e guariti centinaia e centinaia di italiani malati di Covid-19 (l'ultimo, ultrassettantenne, a Genova). E il numero di guariti sale, ogni giorno, nel nostro Paese, toccando oggi quasi il tetto dei 3mila.
A mano a mano sono state intraprese altre strade, come quella dell'antireumatoide impiegato a Napoli e per cui sempre l'Aifa ha dato il via libera alla sperimentazione su ben 330 pazienti. Ecco come agiscono le terapie e i farmaci messi in campo dai medici italiani.
Gli antivirali, la “strada” dello Spallanzani
Si

Gli antinfiammatori, il protocollo di Napoli
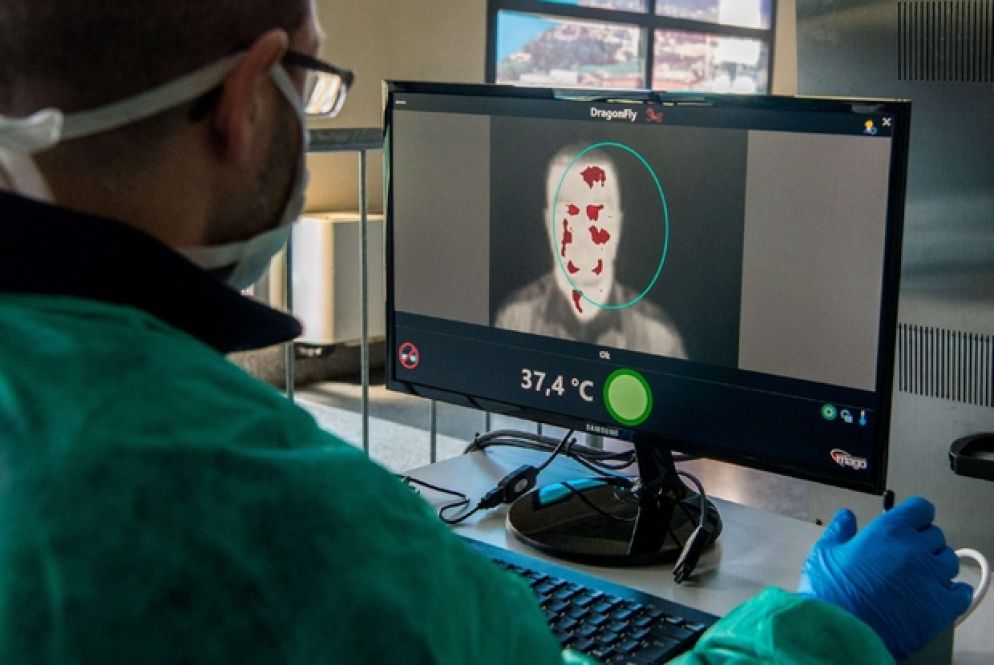
Il plasma dei guariti, la scomessa di Mantova
L'antimalarico, ci crede la Francia
Da anti-malarico ad anti-Covid. Dopo un primo studio cinese, la vecchia clorochina, farmaco contro la malaria ormai “60enne”, è stato testato in Francia su pazienti con coronavirus, con risultati che fanno parlare l'autore della sperimentazione - l'infettivologo Didier Raoult dell'istituto Méditerranée Infection di Marsiglia - di "rivoluzione". Il farmaco infatti, è stato somministrato a 24 pazienti e, dopo soli sei giorni, ben tre quarti dei 24 pazienti non erano più positivi al virus. E ancora: in combinazione con l'antibiotico azitromicina, specifico contro la polmonite batterica, il trattamento ha totalmente guarito i pazienti dopo una settimana, mentre il 90% dei malati che non avevano assunto farmaci era ancora positivo.
La Clorochina avrebbe due effetti per accelerare l'eliminazione del virus, spiega Raoult: modificherebbe prima l'ambiente acido del vacuolo della cellula, un piccolo sacchetto di liquidi protetto dalla membrana che serve da tana per i virus. Aumentando il suo pH, l'equilibrato ecosistema di questo “rifugio” del virus viene ad essere “scombussolato” e viene così impedita l'azione degli enzimi coinvolti nel meccanismo cellulare utilizzato dal virus per replicarsi. I detrattori dello studio sostengono però che questo approccio non abbia il rigore, i protocolli e il numero di pazienti richiesti dai comitati di scientifici, chiamati a valutare l'efficacia di una molecola terapeutica rispetto a un gruppo di controllo placebo. «In assenza di dati clinici importanti e pubblici, non si possono dedurre prove di efficacia e tanto meno elaborare raccomandazioni», riassume Francois Maignen, specialista di Salute pubblica.
Anche per gli antimalarici, in particolare Clorochina, l'Aifa ha dato il via libera all'uso off label in Italia.
Un farmaco specifico in Olanda

Le staminali in Cina
E il vaccino?
È partito in tempi rapidissimi negli Stati Uniti il primo test di un vaccino contro il coronavirus e l'Europa ha annunciato che la sua sperimentazione potrà partire in giugno: la ricerca corre veloce e affina le armi contro un virus mai visto finora, ma nessuno si illude che i tempi saranno brevi. Ci vorrà da un anno a un anno e mezzo per avere il vaccino, mentre la durata della pandemia è ancora
imprevedibile, come indicano anche i dati sui casi in Italia. La ricerca ha mantenuto la sua promessa più grande: a metà febbraio il direttore dell'istituto statunitense per lo studio delle malattie infettive Niaid (National Institute of Allergy and Infectious Diseases) aveva annunciato che entro due o tre mesi sarebbe iniziato il test del vaccino messo a punto con collaborazione con l'azienda Moderna e con la Coalion for Epidemic Preparedness Innovation (Cepi) e puntualmente il vaccino è stato iniettato lunedì 16 febbraio al primo dei 45 volontari sani a Seattle, una donna. È un vaccino a Rna messaggero, ossia un vaccino sintetico, che non utilizza il virus ma la sua informazione genetica. Dopo questa prima fase di test sull'uomo ce ne saranno altre due per avere tutte le risposte necessarie su sicurezza ed efficacia e poi bisognerà aspettare i tempi tecnici per la produzione.
imprevedibile, come indicano anche i dati sui casi in Italia. La ricerca ha mantenuto la sua promessa più grande: a metà febbraio il direttore dell'istituto statunitense per lo studio delle malattie infettive Niaid (National Institute of Allergy and Infectious Diseases) aveva annunciato che entro due o tre mesi sarebbe iniziato il test del vaccino messo a punto con collaborazione con l'azienda Moderna e con la Coalion for Epidemic Preparedness Innovation (Cepi) e puntualmente il vaccino è stato iniettato lunedì 16 febbraio al primo dei 45 volontari sani a Seattle, una donna. È un vaccino a Rna messaggero, ossia un vaccino sintetico, che non utilizza il virus ma la sua informazione genetica. Dopo questa prima fase di test sull'uomo ce ne saranno altre due per avere tutte le risposte necessarie su sicurezza ed efficacia e poi bisognerà aspettare i tempi tecnici per la produzione.
È un vaccino a Rna messaggero anche quello che l'azienda biofarmaceutica CureVac, attiva fra Germania e Stati Uniti, si prepara a sperimentare in giugno. L'annuncio è arrivato dalla Commissione Europea ha annunciato che la CureVac «ha già avviato il suo programma di sviluppo di un vaccino anti Covid-19 e si prevede l'avvio di test clinici a partire da giugno 2020».
© RIPRODUZIONE RISERVATA







