È già un 2024 di grandi scoperte nella lotta al cancro
Italia protagonista nella ricerca. Le ultime novità riguardano i tumori del colon, delle vie biliari, quelli gastrici e la leucemia linfoblastica acuta, che oggi si cura senza chemio

Nuovi farmaci, terapie “chemio-free”, campioni di tumori che diventano modelli tridimensionali. Ben più che speranze, inizia con importanti certezze il 2024 della lotta al cancro. E in gran parte dei casi, l’Italia, che pure non brilla per investimenti in ricerca, gioca ancora un ruolo di primo piano. Vediamo quali sono le ultimissime novità nell’offensiva della scienza alla seconda causa di morte nel mondo occidentale.
Nel microbiota un alleato del tumore del colon-retto
Partiamo da una scoperta delle ultime ore di un gruppo di ricercatori dell’Università di Torino e dell’Istituto fondazione di Oncologia molecolare (Ifom) di Milano, per i quali se alcuni tumori del colon-retto non rispondono alla chemioterapia, che rappresenta ancora oggi un’arma fondamentale per combatterli, è perché ci sono dei batteri intestinali che, “allenando” le cellule maligne, insegnano loro a resistere ai farmaci. Lo studio ha guadagnato la pubblicazione sulla rivista Cell Reports Medicine.
Oggi sono disponibili numerosi farmaci contro questa neoplasia, alcuni dei quali condividono il meccanismo di danneggiare il Dna delle cellule tumorali, sgretolandolo pezzo dopo pezzo, finché il tumore rimane senza “istruzioni” e regredisce. Spesso però questi medicinali colpiscono anche le cellule normali, causando effetti collaterali che possono precludere la prosecuzione del trattamento. E poi, non tutti i tumori intestinali rispondono fin dall'inizio allo stesso farmaco. Da qui la scelta degli scienziati che hanno adottato un cambio di prospettiva innovativo: anziché concentrarsi solo sul tumore, si è preferito studiare ciò che lo circonda, tra cui l'insieme dei batteri che popolano l'intestino: il cosiddetto microbiota.
Lo studio, svolto grazie al sostegno di Fondazione Airc e di un grant dell'Ue, è stato coordinato da Alberto Bardelli, direttore scientifico di Ifom e ordinario dell'Università di Torino: «Il microbiota - ha spiegato - svolge molte funzioni importanti e positive per il nostro organismo, ma ci sono alcuni batteri che promuovono lo sviluppo del cancro. In particolare, una tossina, la colibactina, è stata trovata arricchita in una frazione di tumori colorettali. Ci siamo dunque chiesti se ci potesse essere una correlazione, cioè se l'esposizione alla tossina potesse influenzare il modo in cui i tumori rispondono ai trattamenti».
Nelle parole del primo autore dell’articolo, il ricercatore del dipartimento di Oncologia dell’Università di Torino, Alberto Sogari, i risultati della ricerca: «Abbiamo scoperto che la colibactina funziona come una sorta di “palestra per i tumori”: allena le cellule tumorali a sopportare un carico costante di mutazioni al Dna, abituandole. Così, quando si inizia il trattamento chemioterapico, il cancro impara anche a tollerare il danno provocato dai farmaci, diventando resistente». Gli autori dello studio hanno osservato che anche tumori allenati dalla colibactina possono tuttavia rispondere ad approcci chemioterapici che agiscono con un meccanismo diverso. Fondamentale è dunque «rendere i trattamenti il più possibile precisi e mirati. Abbiamo già ottenuto - ha aggiunto Bardelli - i primi risultati incoraggianti che confermano le ricadute traslazionali della nostra scoperta». L’obiettivo adesso è testare la scoperta su un numero molto maggiore di pazienti.
Tumore gastrico, nuovo farmaco per i casi più gravi
A proposito di tumori addominali e intestinali. A distanza di oltre 10 anni dall’approvazione, nell’Ue, dell’ultimo farmaco per il carcinoma gastrico, l’Aifa (Agenzia italiana del farmaco) ha appena disposto la rimborsabilità di “trastuzumab deruxtecan”. È una monoterapia per trattare pazienti con adenocarcinoma dello stomaco o della giunzione gastroesofagea avanzato, cosiddetto “Her2-positivo”, che hanno ricevuto un precedente trattamento a base di trastuzumab. Nel 2023, in Italia sono stati stimati circa 15mila nuovi casi di tumore dello stomaco (9.000 uomini e 6.000 donne). Il 20% presenta una sovra-espressione della proteina Her2. I pazienti con malattia avanzata metastatica, che sono progrediti dopo un trattamento proprio contro questa proteina, possono ora beneficiare del nuovo farmaco, che combina un anticorpo monoclonale, trastuzumab, con il chemioterapico deruxtecan.
Il ritrovato «ha dimostrato di essere efficace in una condizione clinica complessa, cioè in alcuni pazienti non suscettibili di chirurgia, dopo il fallimento della prima linea di terapia medica - ha detto Sara Lonardi, direttore dell'Oncologia 3 all'Istituto Oncologico Veneto Irccs di Padova -. Per queste persone finora le possibilità di cura erano limitate». Queste cure innovative «rappresentano un passo avanti significativo nel controllo della malattia metastatica - ha sottolineato Claudia Santangelo, presidente dell'associazione pazienti “Vivere senza stomaco (si può)” -. Il tumore gastrico è una patologia ad alta complessità clinica e richiede percorsi dedicati per diagnosi, cura e assistenza. La presa in carico di questi pazienti, in particolare con carcinoma avanzato, necessita di un approccio multidisciplinare che permetta una gestione globale, migliorando la sopravvivenza e la qualità di vita».
Un modello 3D per la ricerca sul tumore delle vie biliari
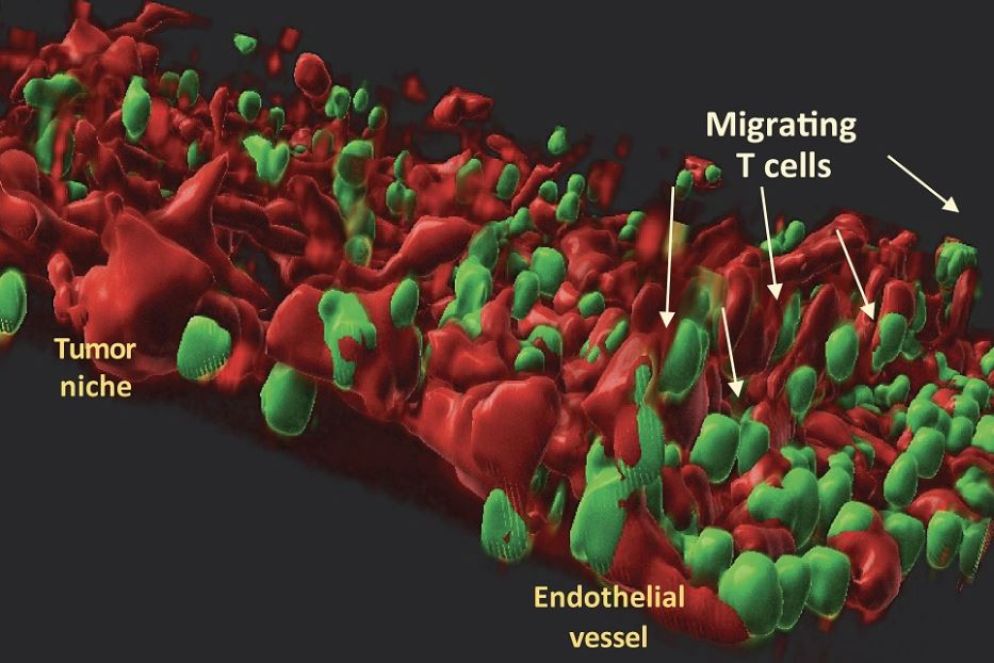
Riguarda invece il cancro delle vie biliari il lavoro dei ricercatori del Politecnico e del Gruppo Humanitas di Milano, che hanno creato un modello 3D di tumore per accelerare ricerca e medicina personalizzata. Un chip di pochi centimetri di grandezza ma che al suo interno nasconde un modello tridimensionale, «altamente fedele», di un tumore raro, il colangiocarcinoma, completo del suo microambiente tumorale. Il modello, specifico per singolo paziente, che si può quindi realizzare a partire da un campione di cellule prelevato dal malato, integra biomedicina, fisica e ingegneria, ed è frutto della sinergia tra Ana Lleo De Nalda, docente di Humanitas University e responsabile del laboratorio di Immunopatologia epatobiliare dell’Irccs Istituto clinico Humanitas, e Marco Rasponi, professore associato di Tecnologie per la medicina rigenerativa al Politecnico di Milano, dove è anche responsabile del laboratorio di Microfluidica e microsistemi biomimetici. Con loro ha collaborato l’équipe del professor Guido Torzilli, direttore del dipartimento di Chirurgia generale e responsabile della Chirurgia epatobiliare di Humanitas.
«L'obiettivo ultimo di questo dispositivo non è solo accelerare la ricerca sul colangiocarcinoma ma anche rendere le cure sempre più precise e mirate, poiché in futuro potrebbe permettere di valutare preventivamente l'efficacia delle terapie in ciascun paziente», hanno evidenziato Lleo e Rasponi. La ricerca è stata finanziata dalla Fondazione Airc e i risultati sono stati pubblicati sul Journal of Hepatology Reports.
Il colangiocarcinoma è un tumore del fegato che colpisce ogni anno circa 5.500 persone in Italia. Purtroppo, la diagnosi avviene spesso in fase avanzata, perché la malattia è spesso asintomatico: al momento della diagnosi solo il 10-30% dei pazienti ha un tumore operabile chirurgicamente. «Proprio per le ridotte opzioni terapeutiche e l'alta mortalità, abbiamo bisogno di nuovi modelli di laboratorio in grado di riprodurre le caratteristiche della malattia. È particolarmente importante l'interazione tra le cellule del tumore e quelle del sistema immunitario, che svolgono un ruolo fondamentale nella progressione e nella risposta ai farmaci», ha rilevato Ana Lleo.
Nel dispositivo è stato riprodotto quanto avviene a livello individuale nei pazienti, sia nella propagazione del tumore sia nella risposta ai farmaci. «Siamo molto felici del risultato ottenuto - hanno commentato Lleo e Rasponi -. I prossimi passi saranno arricchire ulteriormente il dispositivo, sia come modello per la ricerca sia come possibile test farmacologico personalizzato, e testarlo in gruppi più ampi di pazienti».
Stop alla chemio: la svolta nella leucemia linfoblastica
Dai tumori solidi a quelli del sangue. Dati alla mano, adesso si può affermare che la storia clinica della leucemia acuta linfoblastica, nel sottogruppo “Philadelphia positiva” (Lal Ph+), è cambiata. Grazie a un trattamento di prima linea basato sull'uso combinato di due farmaci che agiscono in modo mirato, senza il ricorso a chemioterapia e trapianto di staminali. Ad oltre 4 anni dalla diagnosi, uno studio targato Gimema (Gruppo italiano malattie ematologiche dell'adulto), coordinato da Robin Foà della Sapienza Università di Roma, ne ha confermato l'efficacia a lungo termine. I risultati del lavoro sono pubblicati sul Journal of Clinical Oncology.
La “Lal Ph+” è il sottogruppo più frequente di questo tumore ematologico con un'incidenza che aumenta con l'età. In passato era considerata il tumore del sangue con il decorso più infausto, perché poco rispondente alla chemio. L'unica strategia potenzialmente curativa era il trapianto allogenico di cellule staminali, raramente percorribile per la scarsa sensibilità alla chemio e per l'età avanzata di molti pazienti. La prognosi è cambiata dall'inizio degli anni 2000 con l'introduzione nella pratica clinica degli inibitori delle “tirosin-chinasi”, mirati alla lesione genetica che caratterizza la “Lal Ph+”. Associati alla terapia steroidea senza chemio, si sono osservate percentuali molto elevate di remissioni cliniche e limitati effetti collaterali, in pazienti di tutte le età. Gli inibitori delle tirosin-chinasi, inoltre, sono somministrati per via orale e quindi spesso a domicilio, con un vantaggio per la qualità di vita dei pazienti.
Successivamente, il gruppo guidato da Foà ha utilizzato un inibitore di seconda generazione (dasatinib), seguito da un trattamento di consolidamento con un anticorpo monoclonale (blinatumomab) in grado di riconoscere due antigeni, uno sulle cellule tumorali e uno sui linfociti che sono così attivati contro il tumore. L'uso congiunto dei due farmaci ha permesso di ottenere una remissione completa della leucemia nel 98% dei pazienti, di tutte le età, senza effetti collaterali rilevanti. I risultati dello studio Gimema, sostenuto anche in questo caso da Fondazione Airc e con il contributo di Amgen, sono stati pubblicati nel 2020. Ora dallo stesso team sono arrivati i dati di oltre 4 anni di follow-up (53 mesi), che confermano l'efficacia di questa strategia con percentuali di sopravvivenza tra il 75% e l'80%. Lo studio ha anche mostrato che il 50% dei pazienti è stato trattato con la sola terapia combinata, senza dover ricorrere a chemio o trapianto. Nessuno dei pazienti con risposta molecolare profonda precoce ha presentato recidive.
«Questi risultati - ha affermato Foà, professore emerito di Ematologia alla Sapienza - sono i migliori fino ad oggi ottenuti, perché si sono mantenuti nel tempo e a prescindere dall'età dei pazienti. È la strategia che rappresenta il futuro: chemioterapia e trapianto potranno dunque essere evitati in moltissime persone». Quest'ultimo punto, ha fatto sapere l’ateneo romano, verrà definitivamente documentato dal nuovo protocollo clinico multicentrico Gimema di fase 3, attualmente in corso in Italia.
© RIPRODUZIONE RISERVATA






