La ricerca italiana ha nuove armi contro i due tumori killer
Dai farmaci preoperatori che migliorano la sopravvivenza nel cancro del pancreas, alla scoperta del segreto dell'immortalità delle cellule neoplastiche del cervello: così si ridisegnano le terapie
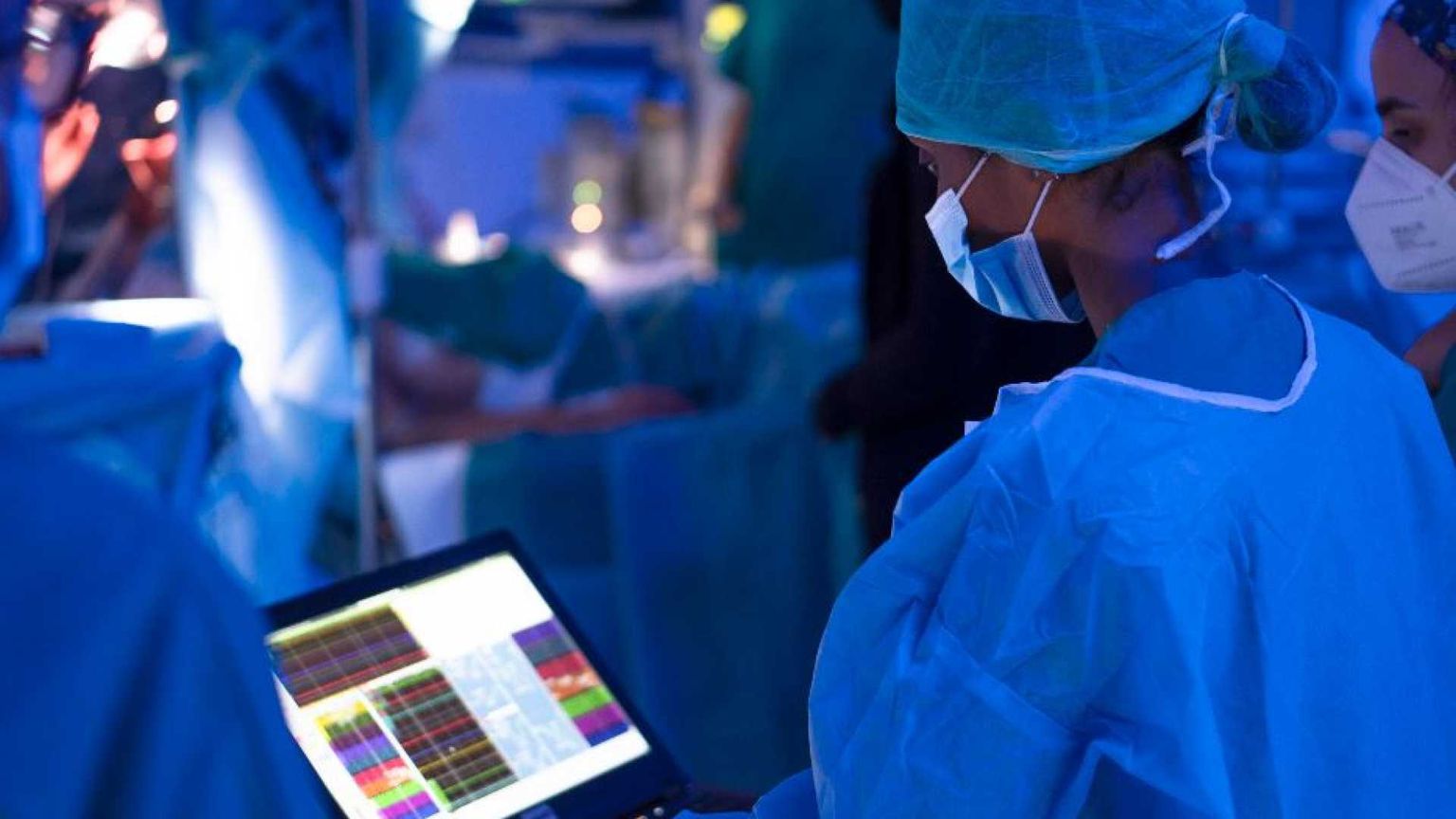
Pancreas e cervello, ovvero i “santuari inviolati” dove il cancro si sviluppa e prolifera quasi indisturbato, e dove le attuali terapie possono poco o nulla. È proprio contro l’adenocarcinoma duttale (il tumore del pancreas) e il glioblastoma (cervello) che arrivano però importanti novità dalla ricerca.
Pancreas, un trattamento che cambia le linee guida
Andiamo con ordine. L’ultima in ordine di tempo è degli scienziati dell’Irccs Ospedale San Raffaele di Milano, che hanno appena presentato al più importante congresso mondiale di oncologia, l’Asco di Chicago, i risultati dello studio di fase 3 “Cassandra”, che ha coinvolto 17 ospedali italiani, e che è finalmente destinato a cambiare le linee guida per il trattamento del tumore del pancreas. I ricercatori, coordinati da Michele Reni, primario di Oncologia e associato all’Università Vita-Salute San Raffaele, hanno dimostrato che trattare i pazienti con malattia non metastatica - e quindi candidati all’intervento chirurgico -, con una combinazione di farmaci chemioterapici (Paxg) creata al San Raffaele nel 2012 (e autorizzata dall’Aifa nel 2020), migliora la sopravvivenza libera da eventi sfavorevoli rispetto al trattamento standard “mFolfirinox”.
Lo studio ha arruolato 260 pazienti. Quelli trattati con Paxg hanno dimostrato una sopravvivenza senza eventi sfavorevoli (progressione, recidiva, inoperabilità, aumento progressivo dei marcatori, riscontro di metastasi durante l’intervento, decesso) «significativamente più lunga». Tanto da autorizzare il professor Reni a parlare di «un passo storico nella lotta contro questo tumore, per l’entità della differenza osservata rispetto a quello che, fino ad oggi, veniva considerato da molti lo schema terapeutico più efficace». Risultati che, per il co-responsabile dello studio, Massimo Falconi, primario della Chirurgia del pancreas e ordinario di Chirurgia in Vita-Salute San Raffaele, «aprono la strada a un possibile aggiornamento delle linee guida».
L’adenocarcinoma duttale rappresenta il 95% di tutte le neoplasie pancreatiche maligne. Ogni anno costituisce circa il 3% dei nuovi casi di cancro, è la terza principale causa di morte oncologica e presenta il peggior tasso di sopravvivenza a 5 anni tra i tumori solidi. Viene spesso diagnosticato in fase avanzata e solo il 10-20% dei pazienti è candidabile alla chirurgia. Tuttavia, in oltre il 90% dei pazienti con malattia apparentemente localizzata al pancreas, sono presenti metastasi microscopiche, non documentabili con gli strumenti diagnostici esistenti. Uno degli aspetti singolari dello studio Cassandra è di essere stato interamente finanziato da 5 associazioni di pazienti: My Everest, Codice Viola, Associazione per la vita, Natalucci e Oltre la Ricerca. Lo studio prosegue ora per stabilire la durata ottimale della chemioterapia preoperatoria.
Così si aggira la resistenza del glioblastoma
Dal pancreas al cervello. Anche qui le novità sono importanti. Perché l’Irccs Istituto europeo di oncologia (Ieo) di Milano ha svelato il “segreto di immortalità” delle cellule immature (dette “Tics”) che, dribblando le cure e continuando ad alimentare la malattia, sono responsabili dell’insorgenza e del mantenimento del glioblastoma. Ebbene, in modelli preclinici, i ricercatori Ieo hanno trovato una nuova via per eludere la resistenza di questo tumore ai farmaci e rendere le terapie più efficaci. Il lavoro, sostenuto da Fondazione Airc e pubblicato su Science Advances, è coordinato da Giuliana Pelicci, direttrice dell'unità di ricerca del dipartimento di Oncologia sperimentale Ieo e professoressa di Biologia molecolare dell'Università del Piemonte Orientale.
Ogni anno in Italia si stimano circa 1.500-2mila diagnosi di glioblastoma, con una mortalità che resta molto alta. Il nuovo studio è la continuazione di una ricerca precedente, in cui lo stesso gruppo di scienziati ha dimostrato che l'inibizione di un enzima, chiamato “Lsd1”, tramite l'impiego del composto sperimentale “Lsd1i”, può avere un impatto significativo sul trattamento del glioblastoma, colpendo le cellule-serbatoio Tics. «I nostri nuovi risultati - illustra Pelicci - dimostrano che non tutte le Tics di glioblastoma risultano sensibili a Lsd1i: alcune riescono ad adattarsi e sopravvivere attivando specifici processi metabolici. Abbiamo allora identificato i geni coinvolti in vie metaboliche fondamentali, che potrebbero rappresentare bersagli terapeutici alternativi o complementari a Lsd1i». Alcuni di questi geni sono già oggetto di sperimentazioni cliniche. «Siamo in una fase preclinica - aggiunge Pelicci - ma è un passo avanti significativo nella lotta a un male ancora privo di cure risolutive».
L'Intelligenza artificiale svela le metastasi
Cure per le quali sta prepotentemente entrando in gioco l’Intelligenza artificiale (Ia) anche in presenza di metastasi cerebrali. Qui i progressi sono firmati da un’altra eccellenza milanese, l’Irccs Istituto clinico Humanitas, in collaborazione con l’University Hospital di Tubinga (Germania). Un gruppo di ricerca coordinato da Letterio Politi, responsabile della Neuroradiologia, e da Marta Scorsetti, responsabile di Radioterapia e Radiochirurgia, entrambi docenti di Humanitas University, ha dimostrato l’efficacia dell’Ia nel distinguere tra le alterazioni indotte dalla radioterapia del tessuto cerebrale e la progressione del tumore. Una possibilità che potrebbe facilitare, e di molto, le scelte terapeutiche. Le tecniche diagnostiche convenzionali, infatti, come la Risonanza magnetica, spesso non aiutano perché le caratteristiche radiologiche dei due tipi di tessuto sono simili. Ma secondo i risultati di questa ricerca, pubblicata su Neuro-Oncology, con l'Ia si concretizza la possibilità di superare questi limiti. I ricercatori hanno analizzato retrospettivamente 124 lesioni cerebrali in pazienti sottoposti a radioterapia stereotassica, e si sono avvalsi della radiomica e di algoritmi di Ia, grazie ai quali è stato possibile distinguere «con elevata accuratezza» la radionecrosi dalla progressione tumorale, tanto da ridurre la necessità di biopsie o procedure chirurgiche esplorative.
Novità anche per il colon-retto metastatico
A proposito di metastasi. Quelle al fegato derivanti dal tumore del colon-retto (tra le principali cause di morte tra i pazienti oncologici) potrebbero essere trattate presto da una nuova immunoterapia: cellule Car-T progettate per colpire selettivamente il tumore. La ricerca, appena pubblicata su Science Translational Medicine e coordinata da Monica Casucci, responsabile del laboratorio di ricerca Immunoterapie innovative dell’Ospedale San Raffaele di Milano, può rappresentare una svolta per questa patologia, visto che le attuali terapie non sono risolutive nella maggior parte dei casi. Le Car-T ingegnerizzate riconoscono una proteina, la “Caderina-17” (Cdh17), presente in grandi quantità sulle cellule tumorali e assente o non accessibile nei tessuti sani. Gli esperimenti condotti su modelli preclinici hanno dimostrato che le Car-T “addestrate” bloccano efficacemente la crescita del tumore senza danneggiare i tessuti normali. Il prossimo passo? «Una sperimentazione clinica di fase 1-2 per valutare la sicurezza e l’efficacia sui pazienti», afferma Monica Casucci. Non solo: «I risultati potrebbero aprire nuove prospettive terapeutiche anche per altri tumori, come quello dello stomaco e i tumori neuroendocrini».

Lo studio, condotto in collaborazione con l’Institut Cochin dell’Università “Paris-Cité”, si inserisce nel programma di ricerca 5xmille, iniziato 6 anni fa che beneficia del contributo di Fondazione Airc e coinvolge 17 gruppi di ricerca e unità cliniche dell’Università Vita-Salute e Ospedale San Raffaele. «La traslazionalità è da sempre la caratteristica che contraddistingue il San Raffaele: mettere a disposizione dei pazienti oncologici competenze cliniche e di ricerca di elevata qualità specialistica e contribuire al progresso della conoscenza scientifica e alla sua applicazione nella pratica quotidiana», evidenzia Fabio Ciceri, direttore del Comprehensive Cancer Center, primario di Ematologia e trapianto di midollo osseo dell’ospedale milanese e ordinario di Ematologia in Vita-Salute.
© RIPRODUZIONE RISERVATA







